Como Espermiogénesis La fase de transformación de las espermátidas creadas por la espermatogénesis en espermatozoides maduros y fértiles se llama. Durante la espermiogénesis, las espermátidas pierden gran parte de su citoplasma y se forma el flagelo, que se utiliza para la locomoción activa. En la cabeza con el ADN nuclear, frente al punto de unión de los flagelos, se forma el acrosoma, que contiene enzimas que le permiten penetrar en el óvulo.
¿Qué es la espermogénesis?

A diferencia de la espermatogénesis, en el curso de la cual las células germinales atraviesan una mitosis y una división de madurez (meiosis) I y II y luego se denominan espermátidas, la espermatogénesis solo afecta la conversión de las espermátidas en espermatozoides maduros y fertilizables.
La espermiogénesis de una espermátide tarda unos 24 días. Las espermátidas, que solo tienen un juego de cromosomas haploides debido a la meiosis anterior, se convierten en una célula especializada que tiene el único propósito de penetrar un óvulo femenino fértil.
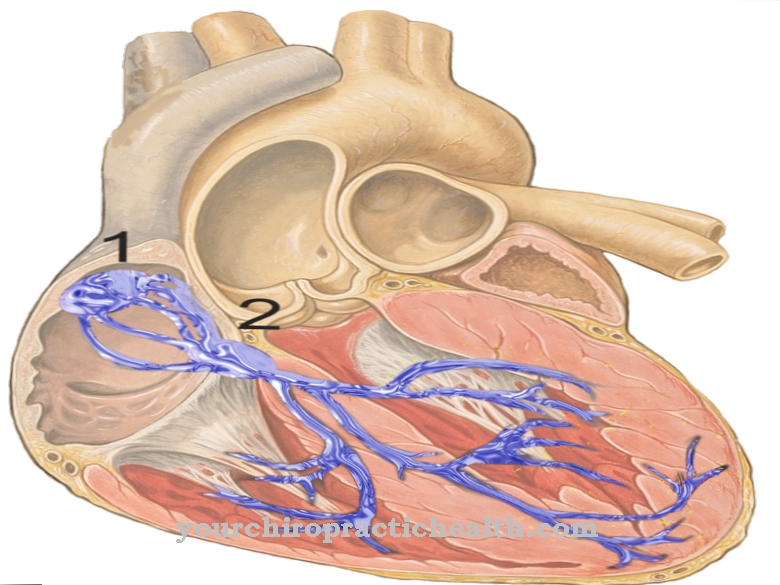
La transformación de una espermátide en un espermatozoide está asociada con cambios internos y externos graves. La espermátide pierde casi todo su citoplasma, por lo que esencialmente solo queda el núcleo, que contiene el ADN. La célula muy reducida se convierte en la cabeza del futuro esperma. Donde se encuentra el centríolo, surge un flagelo, también conocido como cola, que se utiliza para mover activamente los espermatozoides.
En el lado opuesto al flagelo, se forma un casquete, el acrosoma, que contiene enzimas que le permiten penetrar en el huevo femenino. Las mitocondrias, que, incluido su ADN y ARN mitocondrial, estaban ubicadas originalmente en el citosol de la espermátide, se adhieren a la sección media del flagelo y proporcionan la energía necesaria para la locomoción.
Función y tarea
La espermátide, que todavía es reconocible como una célula haploide al comienzo de la espermiogénesis, se transforma en un espermatozoide con grandes cambios externos e internos. El conjunto de cromosomas haploides ya no se modifica. Las mitocondrias simplemente se reubican junto con el ADN y el ARN mitocondriales para dar a los flagelos la energía necesaria para sus movimientos. La única diferencia genética entre los espermatozoides dentro de un eyaculado es que el 50 por ciento contiene un cromosoma X y el otro 50 por ciento contiene un cromosoma Y.
Una característica especial es que el esperma arroja el flagelo cuando penetra en el óvulo femenino y, por lo tanto, el ADN mitocondrial del espermatozoide masculino ya no juega un papel. El ADN mitocondrial del óvulo fertilizado, más tarde el cigoto, proviene exclusivamente de las mitocondrias de la madre.
La espermiogénesis se utiliza para convertir las espermátidas en células de esperma optimizadas y dedicadas. Los espermatozoides fuertes, que pueden moverse lo más rápido posible hacia el óvulo fertilizable después de la eyaculación, tienen más posibilidades de transmitir su conjunto de cromosomas.
Después de acoplarse a la membrana del óvulo, se desencadena un proceso fisiológico que evita que se atraquen más espermatozoides. La capacidad de movimiento y las reservas de energía de los espermatozoides individuales pueden contribuir de manera decisiva a "ganar la carrera".
Se trata menos de la competencia entre los espermatozoides genéticamente idénticos dentro de un eyaculado, sino más de la competencia con el esperma de un eyaculado "extraño", ya que las personas generalmente no viven monógamas. Las posibilidades de ganar la competencia contra "espermatozoides extraños" no se agotan en una "competencia puramente deportiva", pero una parte de los espermatozoides dentro de un eyaculado no puede moverse y puede bloquear virtualmente el camino de los espermatozoides extraños. Dentro de un eyaculado también hay "espermatozoides asesinos", que reconocen los espermatozoides extraños y pueden matarlos con agentes químicos.
Enfermedades y dolencias
Los trastornos, las enfermedades, las anomalías genéticas, el consumo excesivo de alcohol u otras drogas y mucho más pueden conducir a una espermiogénesis deficiente, por lo que puede aparecer una infertilidad reversible o permanente. En la mayoría de los casos, los trastornos de la espermogénesis no deben considerarse de forma aislada, ya que suelen ser el resultado de una espermatogénesis alterada.
En principio, la espermiogénesis alterada puede ser causada por enfermedades o lesiones en los órganos que producen los espermatozoides, los testículos o por disfunciones en la producción de hormonas. Una amplia variedad de anomalías testiculares, como testículos no descendidos, hipoplasia testicular e infecciones de la próstata, así como inflamación testicular relacionada con las paperas (orquitis de las paperas) son causas típicas de trastornos en la espermiogénesis y la espermatogénesis, que generalmente conducen a una fertilidad reducida o incluso a una infertilidad completa.
Enfermedades de los testículos como varicoceles, espermatoceles, hidroceles o tumores de próstata pueden tener efectos similares. La radioterapia para el tratamiento del cáncer, que puede dañar los testículos, también se incluye dentro del rango de trastornos de la espermiogénesis por los órganos productores.
Las enfermedades que pueden afectar la espermatogénesis y la espermiogénesis se consideran causas extragenitales. Son principalmente las infecciones febriles las que pueden alterar temporalmente la formación de espermatozoides como resultado de un aumento de la temperatura en los testículos. Las toxinas ambientales y el manejo relacionado con el trabajo de sustancias tóxicas como el bisfenol A, solventes orgánicos, pesticidas, herbicidas, metales pesados, plastificantes en plásticos y mucho más, presentan riesgos de alteración de la espermiogénesis.
El hipotálamo y la glándula pituitaria, el principal centro de control para controlar los procesos hormonales en el cuerpo, también merecen una atención especial. Si la glándula pituitaria no puede proporcionar hormonas de control como FSH (hormona estimulante del folículo) y LH (hormona luteinizante) y algunas otras en la concentración necesaria, el resultado es una producción alterada, en su mayoría reducida, de hormonas sexuales y por lo tanto a una interrupción de la espermiogénesis.









.jpg)



.jpg)