Homocisteína es un alfa-aminoácido no proteinogénico que contiene azufre, que se forma como un intermedio de la metionina al liberar el grupo metilo (-CH3).
Para el procesamiento posterior de la homocisteína, es necesario un suministro adecuado de vitaminas B12 y B6, así como ácido fólico o betaína como proveedor de grupos metilo. Una mayor concentración de homocisteína en el plasma sanguíneo se asocia con daño a las paredes de los vasos sanguíneos, demencia y depresión.
¿Qué es la homocisteína?
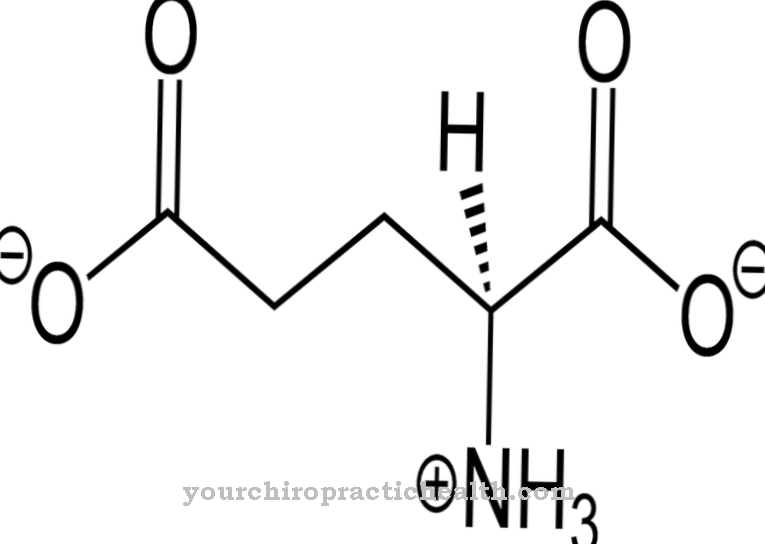
La homocisteína en su forma L bioactiva es un aminoácido no proteinogénico. No puede ser un componente básico de una proteína porque tiende a formar un anillo heterocíclico que no permite un enlace peptídico estable debido a su grupo CH2 adicional en comparación con la cisteína.
Por tanto, la incorporación de homocisteína a una proteína provocaría que la proteína se descompusiera pronto. La fórmula química C4H9NO2S muestra que el aminoácido consiste exclusivamente en sustancias que están disponibles en abundancia en casi todas partes. Los oligoelementos, minerales raros y metales no son necesarios para su estructura. La homocisteína es un ion híbrido porque tiene dos grupos funcionales, cada uno con una carga positiva y una negativa, que en general están equilibrados eléctricamente.
A temperatura ambiente, la homocisteína es un sólido cristalino con un punto de fusión de alrededor de 230 a 232 grados Celsius. El cuerpo puede descomponer un nivel elevado de homocisteína en la sangre formando un puente disulfuro entre dos moléculas de homocisteína para formar homocistina y excretarlas en esta forma a través de los riñones.
Función, efecto y tareas
La tarea y función más importante de la L-homocisteína es apoyar la síntesis de proteínas y convertirse en S-adenosilmetionina (SAM) en cooperación con algunas coenzimas. Con tres grupos metilo (-CH3), SAM es el donante de grupos metilo más importante en el metabolismo celular.
SAM participa en muchas reacciones de biosíntesis y desintoxicación. Los grupos metilo de ciertos neurotransmisores como la adrenalina, la colina y la creatina provienen del SAM. Después de que se ha liberado un grupo metilo, SAM se convierte en S-adenosilmetionina (SAH), que se convierte nuevamente en adenosina o L-homocisteína nuevamente por hidrólisis. Tan importante como es la función de apoyo de la homocisteína para ciertos procesos metabólicos, también es importante que la homocisteína, como producto intermedio de estas cadenas de reacción y síntesis bioquímicas, no se presente en concentraciones anormales en la sangre porque luego desarrolla efectos dañinos.
Por lo tanto, el exceso de homocisteína, que no se requiere para sustentar las conversiones descritas anteriormente en el metabolismo de la metionina, normalmente se descompone aún más con la participación de vitamina B6 (piridoxina) y se excreta a través de los riñones después de que se haya formado la homocistina. Para que la homocisteína pueda cumplir con sus tareas metabólicas, es importante suministrar al organismo cantidades suficientes de vitaminas B6, B12 y ácido fólico.
Educación, ocurrencia, propiedades y valores óptimos
La homocisteína se produce en el cuerpo como un producto intermedio de corta duración dentro del complejo metabolismo de la metionina. La designación alternativa de ácido (S) -2-amino-4-mercaptobutanoico indica la estructura de la homocisteína. Por tanto, es un ácido monocarboxílico con el grupo carboxi característico (-COOH) y al mismo tiempo un ácido graso simple. La homocisteína no se absorbe a través de los alimentos, solo se produce temporalmente en el cuerpo.
Aunque la L-cisteína bioactiva juega un papel importante en la síntesis de proteínas y en la formación de SAM, la concentración óptima y al mismo tiempo tolerable en la sangre está dentro de límites estrechos de sólo 5 a 10 µmol / litro. Los niveles más altos de homocisteína indican ciertos trastornos metabólicos y conducen al cuadro clínico de hiperhomocisteinemia. Es probable que una concentración óptima del aminoácido dependa de la actividad física y mental respectiva y sea difícil de definir. La definición de un límite superior tolerable para el nivel de homocisteína, que debería rondar los 10 µmol / litro, parece más sensata.
Enfermedades y trastornos
Si la concentración de homocisteína excede el límite tolerable, existen principalmente trastornos metabólicos adquiridos o determinados genéticamente en el equilibrio de metionina.
A menudo, solo faltan las vitaminas B6 (piridoxina), B9 (ácido fólico) y B12 (cobalamina) necesarias como coenzimas o catalizadores dentro de la cadena de conversión bioquímica. Se conocen un total de unas 230 mutaciones genéticas, aunque raras, que conducen a una interrupción del metabolismo de la metionina. El aumento patológico de homocisteína se llama homocistinuria. La mutación genética más común que causa la enfermedad se encuentra en el locus del gen 21q22.3. La mutación es autosómica recesiva y provoca la formación de una enzima defectuosa que se requiere para el proceso de descomposición y conversión de la homocisteína.
Las mutaciones previamente conocidas son la omisión (deleción) o la adición (inserción) de nucleobases en las correspondientes cadenas de ADN. Las condiciones de vida y los hábitos desfavorables también pueden causar un aumento de los niveles de homocisteína. Estos incluyen el consumo excesivo de alcohol, el abuso de nicotina, el sobrepeso y el estilo de vida sedentario. Un nivel excesivo de homocisteína puede dañar el endotelio, la pared interna de los vasos sanguíneos y B. Promover la arteriosclerosis. Las venas se vuelven inelásticas y causan una serie de enfermedades secundarias como la hipertensión arterial. También albergan el riesgo de formar trombos, que causan enfermedades coronarias y accidentes cerebrovasculares.
Las enfermedades neurológicas como la depresión y la demencia senil también están asociadas con un aumento del nivel de homocisteína. Los síntomas de la enfermedad son muy diferentes en los niños que padecen homocistinuria genética. El espectro de síntomas va desde las características de la enfermedad apenas detectables hasta la aparición de casi todos los síntomas posibles. Los primeros síntomas generalmente solo aparecen después de los dos años. A lo sumo, se puede observar una ralentización del desarrollo psicomotor durante los dos primeros años de vida. En muchos casos, el primer síntoma de la homocistinuria genética es un prolapso del cristalino del ojo.


.jpg)