A Serina es un aminoácido que es uno de los veinte aminoácidos naturales y no es esencial. La forma D de la serina actúa como coagonista en la señalización neuronal y puede desempeñar un papel en diversas enfermedades mentales.
Que es la serina
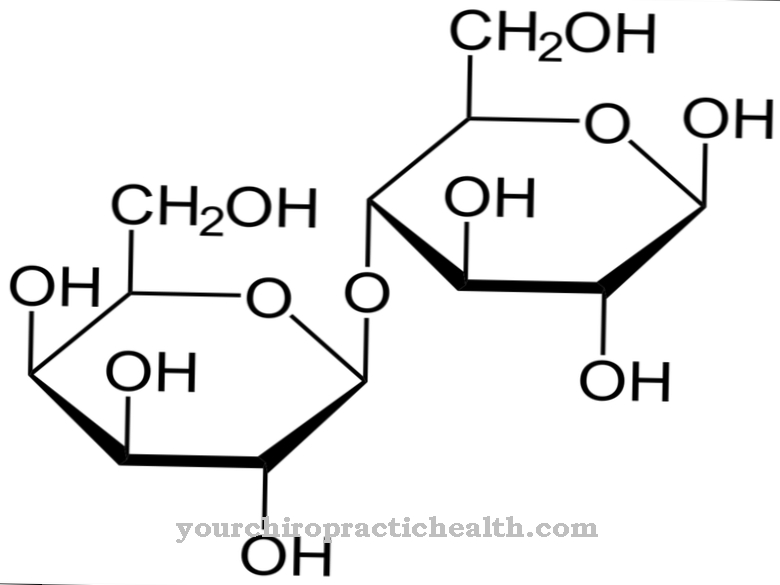
La serina es un aminoácido con la fórmula estructural H2C (OH) -CH (NH2) -COOH. Se presenta en forma de L y es uno de los aminoácidos no esenciales, ya que el cuerpo humano puede producirlo por sí mismo. La serina debe su nombre a la palabra latina "sericum", que significa "seda".
La seda puede servir como materia prima para la serina procesando técnicamente la sericina del pegamento de seda. Como todos los aminoácidos, la serina tiene una estructura característica. El grupo carboxilo consta de la secuencia atómica carbono, oxígeno, oxígeno, hidrógeno (COOH); el grupo carboxilo reacciona ácida cuando se separa un ion H +. El segundo grupo de átomos es el grupo amino. Está compuesto por un átomo de nitrógeno y dos átomos de hidrógeno (NH2).
En contraste con el grupo carboxilo, el grupo amino tiene una reacción básica en el sentido de que une un protón al par solitario de electrones en el nitrógeno. Tanto el grupo carboxilo como el grupo amino son iguales para todos los aminoácidos. El tercer grupo de átomos es la cadena lateral, a la que los aminoácidos deben sus diversas propiedades.
Función, efecto y tareas
La serina tiene dos funciones importantes para el cuerpo humano. Como aminoácido, la serina es un componente básico de las proteínas. Las proteínas son macromoléculas y forman enzimas y hormonas, así como sustancias básicas como la actina y la miosina que forman los músculos.
Los anticuerpos del sistema inmunológico y la hemoglobina, el pigmento rojo de la sangre, también son proteínas. Además de la serina, hay otros diecinueve aminoácidos que se encuentran en las proteínas naturales. La disposición específica de los aminoácidos crea largas cadenas de proteínas. Debido a sus propiedades físicas, estas cadenas se pliegan y forman una estructura espacial tridimensional. El código genético determina el orden de los aminoácidos dentro de dicha cadena.
La mayoría de las células humanas contienen serina en su forma L. Por el contrario, la D-serina se produce en las células del sistema nervioso: las neuronas y las células gliales. En esta variante, la serina actúa como coagonista: se une a los receptores de las células nerviosas y, por lo tanto, activa una señal en la neurona que transmite como un impulso eléctrico a su axón y la envía a la siguiente célula nerviosa. De esta manera, la transferencia de información tiene lugar dentro del sistema nervioso.
Sin embargo, una sustancia mensajera no puede unirse a cada receptor a voluntad: según el principio de bloqueo y llave, los neurotransmisores y los receptores deben tener propiedades que coincidan entre sí. La D-serina se produce, entre otras cosas, como coagonista en los receptores NMDA. Aunque la serina no es la principal sustancia mensajera allí, tiene un efecto reforzador sobre la transmisión de señales.
Educación, ocurrencia, propiedades y valores óptimos
La serina es esencial para el funcionamiento del organismo. Las células humanas forman serina oxidando y aminando 3-fosfoglicerato, es decir, añadiendo un grupo amino. La serina es uno de los aminoácidos neutros: su grupo amino tiene un valor de pH equilibrado y, por tanto, no es ni ácido ni básico. Además, la serina es un aminoácido polar.
Dado que es uno de los componentes básicos de todas las proteínas humanas, es muy común. La serie L es la variante natural de la serina y se presenta principalmente a un pH neutro de alrededor de siete. Este valor de pH prevalece dentro de las células del cuerpo humano, en las que se procesa la serina. La L-serina es un ion híbrido. Un zwiterión se forma cuando el grupo carboxilo y el grupo amino reaccionan entre sí: el protón del grupo carboxilo migra al grupo amino y allí se une al par de electrones libres.
El zwitterión tiene una carga tanto positiva como negativa y no está cargado en su conjunto. El cuerpo a menudo descompone la serina en glicina, que también es un aminoácido que, como la serina, es neutral pero no polar. La serina también puede producir piruvato, que también se conoce como ácido acetilfórmico o ácido pirúvico. Es un ácido cetocarboxílico.
Enfermedades y trastornos
En su forma L, la serina se encuentra en neuronas y células gliales y probablemente desempeña un papel en diversas enfermedades mentales. La L-serina se une como coagonista a los receptores de N-metil-D-aspartato, o receptores NMDA para abreviar. Refuerza el efecto del neurotransmisor glutamato, que se une a los receptores NMDA y, por tanto, activa las células nerviosas.
Los procesos de aprendizaje y memoria dependen de los receptores NMDA; indica la remodelación de las conexiones sinápticas y, por lo tanto, cambia la estructura del sistema nervioso. Esta plasticidad se expresa como aprendizaje a nivel macro. La ciencia considera que esta conexión es relevante para las enfermedades mentales. Las enfermedades mentales conducen a numerosos impedimentos funcionales, que a menudo también incluyen problemas de memoria. Los procesos de aprendizaje defectuosos también pueden contribuir al desarrollo de enfermedades mentales. Un ejemplo de esto es la depresión. La depresión conduce a un rendimiento cognitivo deficiente, especialmente cuando es muy grave. Sin embargo, la capacidad de aprender y la memoria mejoran nuevamente cuando la depresión cede.
Una teoría actual asume que la activación frecuente de determinadas vías nerviosas aumenta la probabilidad de que estas vías se activen más rápidamente en caso de futuros estímulos: el umbral de estímulo desciende. Esta consideración se basa en un desbloqueo de los receptores, lo que podría explicar el proceso. En el caso de enfermedades mentales como la depresión o la esquizofrenia, puede haber una interrupción en este proceso, lo que puede explicar al menos parte de los síntomas respectivos. En este contexto, los estudios iniciales confirman el efecto de la D-serina como antidepresivo.

.jpg)

.jpg)
.jpg)
.jpg)


.jpg)


.jpg)